中国药品监管部门开始接受境外药品临床试验数据,这一政策调整不仅是医药行业的重大变革,也对包括网络与信息安全软件开发在内的多个领域产生深远影响。这一举措意味着中国在药品审评审批领域与国际标准进一步接轨,旨在加速新药上市、满足患者需求,同时降低本土研发的重复成本。
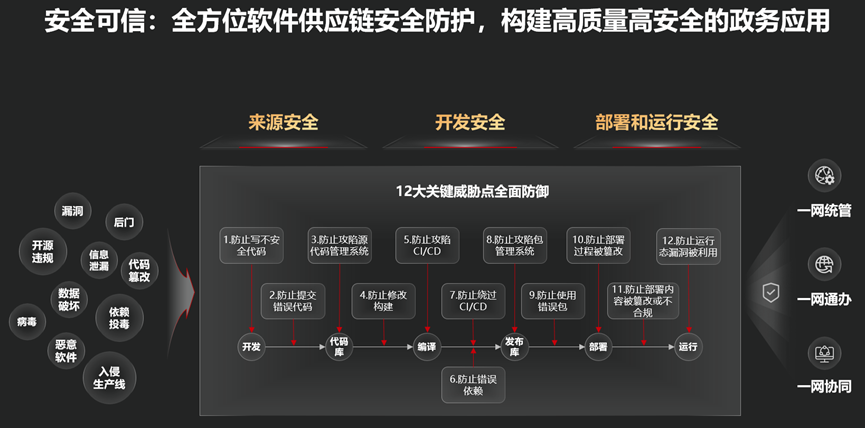
对于网络与信息安全软件开发行业而言,这一变化带来了双重影响。一方面,境外临床试验数据的引入意味着相关数据跨境传输、存储和分析的需求将显著增加。药品试验数据通常包含大量敏感信息,如患者隐私、研发细节等,这些数据的处理必须符合中国《网络安全法》、《数据安全法》和《个人信息保护法》的严格要求。因此,国内信息安全软件开发商将面临新的市场机遇——开发或升级能够保障跨境数据安全流动的解决方案,例如加密传输系统、数据脱敏工具和合规监控平台。
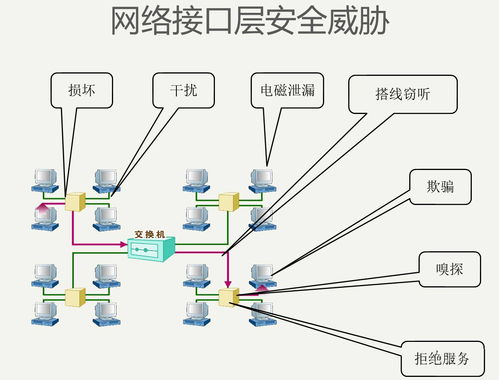
另一方面,这也对信息安全软件的技术水平提出了更高要求。境外数据来源多样,格式和标准可能不统一,需要软件具备强大的数据整合与验证能力,以确保临床试验数据的真实性、完整性和可追溯性。随着国际合作的加深,网络攻击风险可能上升,安全软件需强化防护措施,防止数据泄露或篡改,这包括开发更先进的入侵检测系统和实时威胁响应机制。
从行业生态角度看,这一政策鼓励了跨领域合作。网络信息安全企业可与医药研发机构、数据服务商联手,构建端到端的安全数据管理生态链,推动技术创新。例如,利用区块链技术确保试验数据不可篡改,或应用人工智能进行异常行为分析,都将成为未来发展的重点方向。
中国接受境外药品临床试验数据不仅是医药行业的开放信号,更为网络与信息安全软件开发领域注入了新动力。开发商需抓住机遇,提升产品合规性和技术先进性,以保障数据安全,助力中国在全球医药研发中扮演更积极的角色。